原子と分子は、私たちの周りの物質を構成する基本的な単位ですが、それぞれ異なる特性を持っています。多くの人が「原子とは何か」、「分子との違いは何か」という疑問を抱くことがあるでしょう。原子は、物質の最も小さな単位であり、化学的性質を持つ元素の基本的な部分です。一方、分子は、二つ以上の原子が結合してできた構造体であり、異なる元素の組み合わせによって新しい物質が生成されます。このように、原子と分子の違いは、物質の構成や性質を理解する上で非常に重要です。
原子は、電子、陽子、中性子から構成されています。元素の種類ごとに異なる数の陽子を持つため、原子はそれぞれ異なる性質を示します。例えば、水素原子は一つの陽子を持つのに対し、酸素原子は八つの陽子を持っています。これらの原子が結びつくことで、分子が形成されます。水分子(H₂O)や二酸化炭素分子(CO₂)のように、原子の結合の仕方によって、物質の性質や機能が大きく変わります。このように、原子と分子の関係は物質の科学において中心的なテーマとなっています。
本記事では、原子と分子の基本的な定義から始まり、それぞれの具体的な例や特徴、さらにその間の相互作用について詳しく解説していきます。原子と分子の理解を深めることは、化学だけでなく、さまざまな科学分野においても重要です。興味を持たれた方は、ぜひ読み進めて、これらの基本的な概念について更に探求してみてください。
Contents
原子と分子の基本的な違いとは?
原子と分子は、化学の基本的な構成要素であり、物質の性質を理解するために重要な概念です。それぞれの用語を定義し、その相違点を詳しく説明します。
原子とは
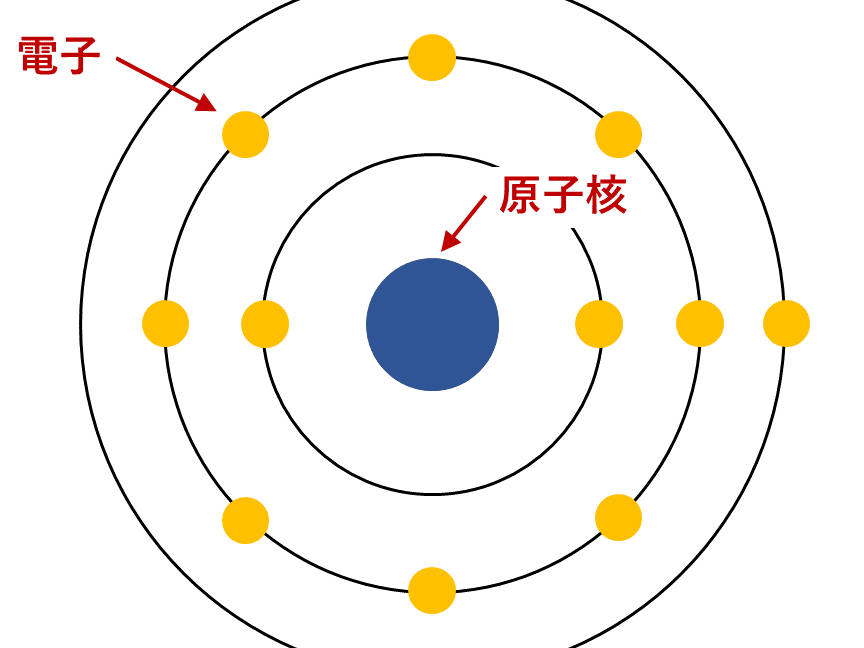
原子は、物質を構成する最小の単位であり、化学的特性を持っています。原子は、中心にある原子核と、それを取り囲む電子から構成されています。原子核はさらに陽子と中性子から成り立っており、これらは原子の質量と元素の特性を決定します。また、原子は周期表において特定の位置に配置されており、元素の種類ごとに異なる原子が存在します。
分子とは
分子は、二つ以上の原子が結合してできた構造体です。分子内の原子は、化学結合(共価結合やイオン結合など)によって結びついており、一つの独立した単位として機能します。分子は、単純なものから複雑なものまで多様であり、水(H₂O)や酸素(O₂)のような小さな分子から、大きなタンパク質やDNAのような高分子まで存在します。
- 原子: 最小の物質の単位。
- 分子: 複数の原子が結合してできる物質の最小単位。
原子と分子の違い
原子と分子の主な違いについて、以下のポイントで説明します。
1. 構成:
– 原子は単一の粒子であり、他の原子と結合することなく存在することもできます。
– 分子は複数の原子が結合したもので、常に他の原子または分子と相互作用しています。
2. 質量:
– 原子の質量はその原子番号に基づいて定義されます。
– 分子の質量は、構成する各原子の質量の合計になります。
3. 性質:
– 原子はそれ自体として特定の化学的性質(例: 金属、非金属)を持つ。
– 分子は新しい性質を示し、異なる属性を持つ場合が多い(例: 水は液体であるが、個々の水素や酸素は気体である)。
4. 安定性:
– 多くの原子は孤立した状態では不安定で、他の原子と結合したいという傾向があります。
– 分子は一般に安定した状態で存在し、必要に応じて外部環境と反応します。
5. 化学反応:
– 原子は直接的に化学反応に関与することは少ないが、反応を通じて新しい分子構造を形成する。
– 分子は化学反応において重要な役割を果たし、新しい分子を生成する際にしばしば変化します。
6. 例:
– 原子の例として、ヘリウム(He)、炭素(C)、鉄(Fe)が挙げられます。
– 分子の例として、水(H₂O)、二酸化炭素(CO₂)、メタン(CH₄)などがあります。
7. 状態:
– 原子は固体、液体、気体の状態でも存在できるが、通常は高エネルギー状態では孤立していることは珍しい。
– 分子も同様に、さまざまな状態で存在できますが、分子の動きとエネルギーレベルが物質の状態に大きく影響します。
8. 記号:
– 各原子は化学記号(例えば、Cは炭素を意味する)で表されます。
– 分子はその構造を示す化学式(例えば、H₂Oは水を意味する)で表されます。
9. 化学結合:
– 原子内の陽子と電子の間には静電的引力があり、これが原子の安定性を保つ。
– 分子内では、原子同士の間に共有電子対や電子を交換することによって化学結合が形成される。
10. 生成プロセス:
– 多くの場合、原子は自然界で直接見られず、他の物質と反応することによって分子が形成される。
– 分子は化学反応の過程で生成され、新しい物質の性質や特性を決定します。
| 特徴 | 原子 | 分子 |
|---|---|---|
| 定義 | 物質の最小単位 | 二つ以上の原子の集まり |
| 構成要素 | 陽子、中性子、電子 | 結合された原子 |
| 質量 | 原子番号に基づく | 構成原子の質量の合計 |
| 安定性 | 時に不安定 | 一般に安定した状態 |
| 化学反応 | 主に反応物として | 化学反応の中心的役割 |
| 例 | 炭素(C) | 水(H₂O) |
| 記号 | 化学記号(例:H、O)</td【実践編】「元素と単体」の納得できる解説【高校化学】原子の世界を覗いてみよう!ー原子構造と電子配置ー原子と分子の違いは何ですか?原子と分子の違いについて説明します。 原子は、物質の最小単位であり、その性質を保持しています。原子は、陽子、中性子、電子から構成されており、元素の種類によって異なる数の陽子を持っています。 一方で、分子は、2つ以上の原子が化学結合によって結びついたものです。分子は、単一の元素からなる場合もあれば、異なる元素が組み合わさった場合もあります。例えば、水(H₂O)は、2つの水素原子と1つの酸素原子から構成される分子です。 したがって、主な相違点は、原子が単一の元素の最小単位であるのに対し、分子は複数の原子が結合してできた構造体であることです。 原子と分子のどちらが小さいですか?原子と分子の相違点について説明します。 原子は物質の基本単位であり、すべての物質を構成しています。原子は、核と呼ばれる中心部に陽子と中性子があり、その周りを電子が回っています。原子の直径は約0.1ナノメートル(1×10^-10メートル)程度です。 一方で、分子は二つ以上の原子が結合したもので、化学的な性質を持ちます。分子は通常、原子よりも大きく、サイズは数オングストロームから数ナノメートルの範囲です。 したがって、全体的に見ると、原子の方が分子よりも小さいということができます。原子が集まって分子を形成するため、原子は分子の構成要素として、より基本的な存在であると言えます。 分子を形成しない原子は何ですか?分子を形成しない原子について考えると、主に単原子ガスとして知られる元素が挙げられます。例えば、希ガス(ヘリウム、ネオン、アルゴンなど)は、分子を形成せずに単独で存在します。これらの原子は、外殻電子が完全であるため、他の原子と結合することがなく、自然界では単体として存在します。 一方で、一般的な元素は、他の原子と結合して分子を形成することが多く、これは化学反応によって行われます。分子は、複数の原子が結合した構造を持ちますが、希ガスはその特性から分子を形成しないという点で特異です。この違いが、分子構造を持つ元素との相違点となります。 元素と原子の違いは何ですか?元素と原子の違いについて説明します。 まず、元素とは、同じ種類の原子が集まってできる物質のことを指します。元素は、周期表において特定の位置を占め、その特性に基づいて分類されます。例えば、酸素(O)や水素(H)などがあります。 一方で、原子は、元素の最小単位であり、物質の基本的な構成要素です。原子は、中心にある原子核と、その周りを回る電子から成り立っています。原子は、化学反応において他の原子と結合したりすることで、分子や化合物を形成します。 要するに、元素は同じ種類の原子の集合体であり、原子は元素の基本単位です。このように、両者は異なる概念ですが、相互に関連しています。 よくある質問 原子とは何ですか?分子とは何ですか? |